【佳学基因检测】肺癌靶向药物基因检测为什么要包含RET重排
肺癌靶向药物基因检测导读:
个性化药物治疗肺癌患者的约来越常见的做法是利用分子靶向药物和免疫检查点抑制剂,这些药物具有良好的治疗反应率和长期预后。迄今为止,美国食品药品监督管理局(FDA)及中国食药局已批准针对表皮生长因子受体(EGFR)突变、间变性淋巴瘤激酶(ALK)融合基因、ROS1、BRAF、MET外显子14跳跃突变、RET融合基因及其相应的分子靶向药物。此外,KRAS突变、EGFR和HER2外显子20插入及其相应的分子靶向药物也经进入基因解码的分析评估范围,并指导药物的选择使用。
然而,在佳学基因等基因解码机构面向公众提供高质量基因检测的之前,患者的治疗可能会在没有检测到罕见突变的情况下进行。据佳学基因肿瘤靶向用药基因检测大数据分析,恶性肿瘤和细胞毒性药物的治疗效果可能因基因突变类型的不同而有所不同。因此,即使是突变阳性的晚期肺腺癌,也可以在不使用分子靶向药物的情况下维持长期的临床进展。特别是在治疗初期成功的情况下,由于在长期存放的情况下,核酸质量会发生改变,前期获得的样本可能不适合进行肿瘤基因面板或者是基因检测包检测。此外,由于病变可能因治疗而发生变化,选择同一位置进行再次活检可能会很困难。佳学基因在案例集中有,在初始诊断七年后再次活检后,通过基因面板检测可检测到RET融合。连续使用分子靶向药物塞尔帕替尼selpercatinib显示出明显的疗效。
肺癌靶向药物塞尔帕替尼
塞尔帕替尼是一种分子靶向药物,属于酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI)的一种。它主要用于治疗某些恶性肿瘤中的特定基因变异,如RET融合基因阳性的肺癌、甲状腺癌和其他实体瘤。
塞尔帕替尼的作用机理是通过抑制肿瘤细胞中的激酶活性,特别是靶向RET激酶。RET是一种酪氨酸激酶受体,在正常情况下参与细胞生长和分化的调控。然而,在某些癌症中,RET基因可能发生融合,导致异常激活和增强的信号传导,促进肿瘤的生长和扩散。塞尔帕替尼通过抑制RET激酶的活性,阻断异常的信号传导通路,从而抑制肿瘤的增殖和生存能力。
塞尔帕替尼具有高度的选择性,主要针对RET激酶,对其他酪氨酸激酶(如EGFR、ALK等)的抑制作用较低。这种高度选择性有助于减少不必要的副作用,并提高治疗的有效性。
总的来说,塞尔帕替尼是一种靶向RET激酶的分子靶向药物,通过抑制异常的信号传导通路,抑制肿瘤的增殖和生存能力,从而在RET融合基因阳性的肺癌、甲状腺癌和其他实体瘤的治疗中显示出显著的疗效。
佳学基因使用过去贮存的肺癌肿瘤进行基因检测并找到靶向药物的启示
很多基因检测机构只进行单基因、单位点突变检测,单基因突变通常通过单重PCR方法进行检测。PCR具有高灵敏度和特异性、快速反应时间和相对较低的成本,主要用于检测EGFR基因的突变,因此得到了广泛应用。然而,随着过去五年来基因解码技术的推广及普及,更多的肺癌驱动基因被发现并且用于研发肿瘤靶向药物。由于时间和样本消耗的限制,依次检测测单个基因突变变得不切实际。早在2014年,佳学基因例便推出了基检测包,临床医院推出基因面板检测,可以同时评估850个以上的癌症相关的基因,类似的基因检测项目在美国也已经出现,并且是美国食品药品监督管理局(FDA)批准的非小细胞肺癌测试中的首批NGS面板之一。然而,高通量肿瘤靶向药物基因检测需要收集组织样本中足够的恶性细胞并经过严格的实验流程进行样本处理。此外,如果样本收集后未经特殊仪器保存,会出现核酸的降解。由于核酸质量的恶化,样本通常不再适合进行基因面板测试。佳学基因的病例中有的初步诊断已超过7年,在假设在这段时间内核酸质量可能已经恶化的情况下,佳学基因进行了原发病灶的再活检。
这是一个罕见的病例,对于原发病灶,细胞毒性化疗和随后的维持治疗非常有效。通常,对于突变阳性晚期肺腺癌,细胞毒性化疗的无进展生存期约为6个月,继续治疗往往很少超过一年。即使在超越疾病进展(beyond-PD)之后继续治疗,在大多数情况下,由于全身性疾病的恶化,不可避免地需要调整治疗方案。没有使用分子靶向药物的具有基因突变的肺腺癌的患者预后通常较差,但也有一些病例在很长时间内观察到肿瘤发展。特别是,据报道,RET融合肺癌显示出较缓慢的临床进展。因此,与佳学基因本例的患者一样,在长期临床过程中使用其他基因检测机构没有检测到罕见突变的病例是存在的。
塞尔帕替尼与其他分子靶向治疗类似,具有足够的全身效应,包括对脑转移的治疗作用。通常,对于基因突变阳性肺腺癌的一线治疗是相应的分子靶向药物;然而,这个案例表明,当通过顺序治疗以追求最长的总生存期时,药物使用顺序可能很重要。在一项针对RET阳性肺癌的3期研究中,将阐明分子靶向药物的疗效,以及与细胞毒性药物的治疗效果。值得注意的是,佳学基因能够从7年前的胸腔积液细胞块中提取RNA,并检测到RET融合,这些细胞块含有较低比例的恶性细胞。
佳学基因肺癌患者临床状况介绍
一名67岁的男性,从未吸烟,无显著病史,因为左侧大量胸腔积液(图1A)被转诊至佳学基因肿瘤基因检测病例交换医院。对左侧胸腔积液进行的细胞学评估显示V级腺癌,与细胞块病理评估一致。使用滑石粉进行胸膜固定后,肺部膨胀良好,左S1 + 2a处出现一颗25×17mm的结节,被认为是原发病灶(图1B)。临床上,他被诊断为腺癌T1cN3M1a,IVA期。初次基因突变筛查进行于七年前,使用其他机构的进行的EGFR突变和ALK免疫组化(IHC)测试结果均为阴性。

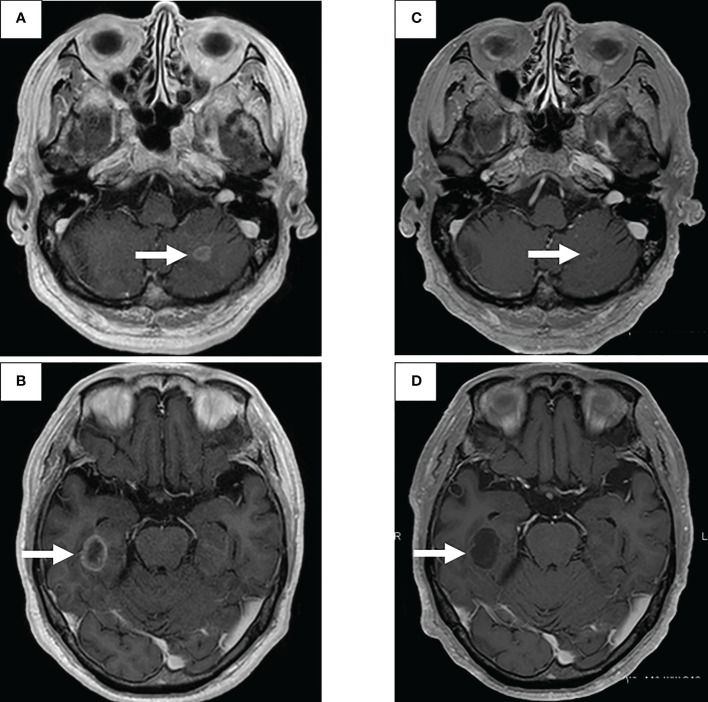
图1:在第一次就诊到开始进行第二次治疗期间,患者7年间原发病灶的顺序图像
一线治疗包括卡铂+培美曲塞+贝伐单抗,经过4个疗程后获得近乎完全缓解(CR),但鼻出血仍然持续,仅进行培美曲塞维持治疗。在维持治疗的25个疗程中实现了CR(图1C),但由于肾功能轻微恶化,治疗暂时中断。治疗结束后一年,CT显示原发病灶轻微进展(图1D),但复发速度较慢。确认CT复发一年后(图1E),重新开始培美曲塞单药治疗,原发病灶和淋巴结减小(图1F)。然而,在进行了32个维持治疗疗程后,出现了快速的全身进展。由于原发病灶再生(图1G)、对侧肺转移、多发性肝转移、右侧肾上腺转移和多发性脑转移(图2A、B),需要调整他的治疗方案。
通过支气管镜对原发病灶进行再活检,细胞学评估显示V级腺癌,组织学评估证实了这一结果。肿瘤精准用药850基因检测确认患者为RET融合基因阳性,随后于第二天给予240mg塞尔帕替尼。第13天的CT显示与基线影像相比(图1H),所有转移病灶,包括脑转移(图2C、D),均有良好的全身反应。由于2级肝酶升高,继续给予剂量减少的塞尔帕替尼(每天160mg)。使用高敏感度的下一代测序(NGS)面板系统:肺癌紧凑面板,并使用细胞学刷液进行RNA检测,证实了融合基因KIF5B外显子15;RET外显子12(K15RET12)。肿瘤精准药基因解码基因检测还能够从7年前的胸腔积液细胞块的福尔马林固定石蜡包埋(FFPE)标本中进一步确认RET(图3A、B),这些标本在恶性细胞的形态学上与再活检样本相似,具有大核仁(图3C、D)。从初始细胞块样本中收集到的RNA(1256ng)具有RNA整合数(RIN)值为4.8。单重PCR和NGS检测均检测到了K15RET12融合峰(图3)。

图3 第一次诊断细胞块的病理学发现显示腺癌,并伴有许多淋巴细胞(A、B,H&E染色,原始放大倍数×400)。再次活检样本显示有肺泡和导管结构的腺癌(C、D,H&E染色,原始放大倍数分别为×200和×400)。通过PCR/NGS检测从第一次诊断标本中检测到了融合KIF5B外显子15;RET外显子12,再活检标本则通过NGS检测。
佳学基因还通过基因检测获得了有关PCR和NGS技术的额外信息。使用SYBR Green实时PCR分析和熔解曲线分析,检测存档的细胞块样本中的RET融合。采用KOD SYBR® qPCR/RT试剂盒(Toyobo)进行逆转录和实时PCR。这些分析按照制造商的方案进行。非肿瘤野生型样本被并行作为阴性对照进行分析。从熔解曲线色谱图中78度的峰值是检测融合阳性的标准。此外,通过对qPCR产物进行NGS测序(Illumina Miseq 150 paired-end),确认了融合边界的序列。
对存档的第一次诊断样本还进行了肺癌紧凑面板检测。从该分析中,也检测到了KIF5b外显子15_RET外显子12融合。从该分析中获得了中等信号强度的融合变异(1,335个总测序读数中的70个融合边界阳性读数)。肺癌紧凑面板检测按照先前描述的方案进行。肺癌紧凑面板对RET融合的检测限度不超过1%的突变等位基因频率。
(责任编辑:admin)


