【佳学基因检测】Na+/H+交换蛋白(NHEs)组分发生突变会引起弱精子症而不育吗?
导读:
男性不育在临床表征是久婚未孕。但实际上却有各种不同的内在原因。基因解码揭示了不同的基因原因导致精子活动在不同阶段不同存面的受损。其中一个原因是精子活化时的钙通道受损引起弱精子症、弱精症。佳学基因在解剖不同的通道蛋白时,揭示精子上的钠氢通道障碍是部分男性不育的原因。而这种原因只有通过基因解码才能清晰地显示出来。
Na+/H+交换蛋白(NHEs)的功能是负责Na+和H+的交换。它们是广泛存在于所有原核生物和真核生物中的膜整合蛋白。NHEs蛋白由SLC9基因家族编码并具有13种不同的钠氢交换蛋白亚型,但在精子细胞中仅存在NHE1、NHE5和sNHE三种亚型。其中,sNHE是参与决定生育力的关键亚型。基因解码发现,在小鼠中敲除NHE1和NHE5基因不会导致小鼠不孕,但是sNHE缺失或sNHE破坏小鼠由于精子的活动性和能动性丧失而变得不育。通过提供氯化铵来提高pH值水平可以恢复部分生育能力,但是cAMP类似物可以完全恢复生育能力。此外,sNHE在蛋白质C末端有核苷酸结合域。因此,sNHE亚型是生育所必需的,环核苷酸可能通过激活sNHE来控制Catsper通道和增加pHi。此外,sNHE有助于维持碱性环境,使Catsper通道进一步调节超极化。除了维持精子的pH值动态平衡外,sNHE还调节精子成熟度,促进上皮细胞对盐和水的吸收。sNHE基因突变导致sNHE的结构和功能发生改变而引起男性不育。因此,靶向sNHE可能是开发新的避孕方法的一个有希望的策略。与Catsper通道一样,sNHE位于精子鞭毛的主要部分,这表明Catsper通道可以感知sNHE的pHi变化来调节Catsper功能。
溶质载体(Solute carriers,SLC),仅次于GPCRs,是脊椎动物中最大的基因家族之一。根据《人的基因序列变化与人体疾病表征》,佳学基因记载了溶质载体蛋白质家族大约450个成员。然而,国际各类数据库对SLC的结构与功能未做深入研究,使得与之相关的基因突变对健康的影响不能采用基因检测的方法进行检测和评估。一个典型的例子是SLC9C1亚家族,也称为sNHE。SLC9C1被怀疑是控制哺乳动物精子细胞内pH(pHi)的Na+/H+交换蛋白。电压感应(VSD)和环核苷酸结合域(CNBD)是用于快速电信号的门离子通道。相比之下,被动地重新分配底物的溶质载体(slc)是由它们的底物本身来控制通道的开放。基因解码研究了精子特异性溶质载体SLC9C1,它具有独特的三元结构:交换域、VSD和CNBD。电压钳荧光分析表明,SLC9C1是一种真正的电压门控Na+/H+交换通道蛋白。细胞信使cAMP改变激活的电压范围。转运域、VSD或CNBD的突变分别强烈影响Na+/H+交换、电压门控或cAMP敏感性。佳学基因的研究揭示SLC9C1是一个结合了溶质载体离子交换机制和离子通道门控机制的经过系统发育进化而的来的嵌合体蛋白。经典的溶质载体通道蛋白缓慢地重新调节细胞内和细胞外环境的变化,而电压门控调节域赋予Na+/H+交换器产生快速pH反应的能力,使下游信号事件发生。与溶质载体不同,SLC9C1的Na+/H+交换通过电压敏感域(VSD)被电压门控,并通过环核苷酸结合域(CNBD)被cAMP直接调控。因此,Na+/H+交换蛋白可以为作为cAMP信号传导的靶点,在pHi和cAMP之间存在适应性相互作用机制。通过了解离子通道和溶质载体之间电压传感和cAMP调制的共性和差异,增加基因突变与临床表征之间关系的准确把握。
与电压激活离子通道一样,SLC9C1通过电压传感器的运动来控制交换通道;这种运动是由cAMP与C末端环核苷酸结合域结合控制的。SLC9C1的VSD在S4基序中含有7个带正电荷的氨基酸。SLC9C1活动是如何由VSD控制的?一般来说,溶质载体是通过在膜两侧通过撞在和释放底物,而引起蛋白质构象的变化。其典型特征是,离子或底物本身会引起蛋白质的构象变化,根据细胞内外底物浓度的变化而被动地实现分配。相反,在SLC9C1中,像VSD这样的通道的运动将膜电压与离子交换耦合起来。
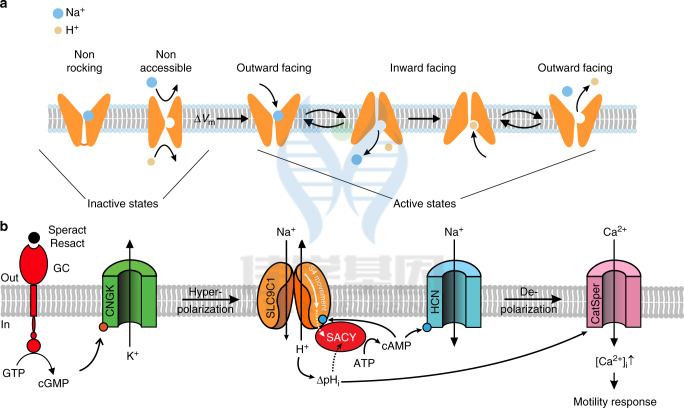
SLC9C1作用是如何受电压和cAMP来控制通道的开关和闭合的?a.SLC9C1只有在电压激活时才激活的示意图。VSD可以通过移除通道上的阻碍构象或增强结合亲和力来提供离子使得通道可以结合离子。或者,在静止状态下,离子可以进入它们的结合位点,但交换转运机制是锁定的(非摇摆);电压解除对转运机制的锁定,从而允许在外向和内向构象之间进行切换。b.海胆精子趋化信号通路。趋化因子结合导致cGMP产生和CNGK通道开放。随后的超极化激活了SLC9C1。碱化和cAMP生产合作打开CatSper通道。说明了交换剂与可溶性腺苷酸环化酶SACY之间的密切相互作用
(责任编辑:admin)


